کپسول آندوسکوپی در یک دههی اخیر از یک ایده جذاب به یک راهکار عملی برای تشخیص بیماریهای گوارشی تبدیل شده و خیلیها آن را قدم اول بهسوی آندوسکوپی بدون درد و عوارض میدانند. در مدلهای رایج، بیمار یک کپسول به اندازهی یک ویتامین بزرگ را میبلعد؛ کپسولی که دوربین و منبع نور دارد و هنگام عبور از روده باریک یا روده بزرگ هزاران تصویر باکیفیت ثبت میکند. این تصاویر بهصورت بیسیم به رکوردر ارسال میشوند و پزشک با کنار هم گذاشتن آنها مسیر گوارشی را مثل یک فیلم کامل میبیند. همین غیرتهاجمی بودن، نبودِ نیاز به بیهوشی یا آرامبخشی، و تجربهی راحت بیمار، آندوسکوپی کپسولی را به گزینهای محبوب در مسیر «مراقبتهای هوشمند و انسانمحور» کرده است.

آندوسکوپی با کپسول – فهیم طب
استاندارد طلایی سالها آندوسکوپی سنتی بوده است؛ روشی ارزشمند که امکان نمونهبرداری و مداخله درمانی را فراهم میکند اما میتواند برای بیمار ناراحتکننده باشد، به آمادگی و امکانات بیشتر نیاز داشته باشد و در برخی موارد دسترسی به تمام بخشهای روده باریک محدود بماند. اینجاست که کپسول آندوسکوپی بهعنوان مکملِ تشخیصی میدرخشد: برای مواردی مثل خونریزی گوارشی پنهان (OGIB)، کمخونی فقر آهن با منشأ نامشخص، بیماری سلیاک، بیماریهای التهابی روده (IBD) و پولیپهای کوچک که در تصویربرداری مقطعی مطرح شدهاند، میتواند مسیر تشخیص را کوتاهتر و دقیقتر کند.
از منظر تجربهی بیمار، مزیتهای کلیدی این روش روشن است: عدم نیاز به لولهگذاری، دوره نقاهت نزدیک به صفر، امکان انجام در محیطهای سرپایی یا حتی تحت پروتکلهای بلع در منزل، و کاهش هزینههای غیرمستقیم (مرخصی از کار، جابهجایی، مراقبت پس از داروهای آرامبخش). از سوی دیگر، پیشرفتهای تکنولوژیک—از بهبود کیفیت اپتیک و باتری تا استفاده از هوش مصنوعی برای «تشخیص کمکیار» (CADx/CAD)—دقت مشاهده ضایعات کوچک را بالا برده و نرخ تصاویر غیرقابلاستفاده را کاهش داده است. نتیجه، افزایش حساسیت و ویژگی تشخیصی در سناریوهای مناسبِ انتخاب بیمار است.
با این حال، برای ترسیم تصویری منصفانه، باید بدانیم آندوسکوپی کپسولی هنوز جایگزین کامل آندوسکوپی مداخلهای نیست. اگر ضایعهای نیاز به نمونهبرداری، برداشتن پولیپ یا هموستاز داشته باشد، همچنان به روشهای سنتی برمیگردیم. گیرکردن کپسول در تنگیها (هرچند نادر) و هزینهی دستگاههای پیشرفته هم از چالشهاست؛ هرچند با «کپسولهای قابلحل»، غربالگری تنگی با کپسولهای تست، و مسیرهای بالینی شفاف، ریسکها مدیریتپذیرتر شدهاند.
آنچه آندوسکوپی کپسولی را به «آیندهی آندوسکوپی» پیوند میدهد، نقشهی راه نوآوریهاست: کنترل مغناطیسی برای هدایت دید، الگوریتمهای AI برای اولویتبندی فریمها و شناسایی ضایعات، افزایش مدتزمان تصویربرداری با باتریهای کممصرفتر، و حتی ایدههای در حال پژوهش مانند بیوپسی مینیاتوری یا دارورسانی هدفمند. این سیر تکامل به معنای تشخیص زودتر، تصمیمگیری سریعتر و تجربهی بیمارمحورتر است.
تاریخچه آندوسکوپی کپسولی داستان عبور از رؤیا به واقعیت است. ایدهی «بلع یک دوربین کوچک برای دیدن داخل روده» دههها مطرح بود، اما محدودیتهای اپتیک، باتری و انتقال داده اجازهی عملیاتیشدن نمیداد. نقطهی عطف در ابتدای دههی ۲۰۰۰ رقم خورد: شرکت Given Imaging با معرفی PillCam نخستین سامانهی تجاری آندوسکوپی کپسولی روده باریک را عرضه کرد و خیلی زود در ایالات متحده تأییدیهی بالینی گرفت. بیمار یک کپسول به اندازهی ویتامین میبلعید؛ دوربین، منبع نور و فرستندهی بیسیم داخل آن تعبیه شده بود و تصاویر به ریکوردر کمربندی منتقل میشد. همین تجربهی غیرتهاجمی و بدون درد و عوارض، کپسول آندوسکوپی را در تشخیص خونریزیهای پنهان روده باریک به گزینهای محبوب تبدیل کرد.
در نسلهای نخست، چالشها کم نبود: کیفیت تصویر پایینتر از اندوسکوپیهای سیمی، عمر باتری محدود، میدان دید و نرخ فریم نهچندان بالا و نبود امکان مداخلهی درمانی. پاسخ صنعت، مسیر تکامل را روشن کرد: افزایش میدان دید، نورپردازی کارآمدتر، نرخ فریم تطبیقی (افزایش فریم در نواحی مشکوک و کاهش در نواحی کمخطر برای صرفهجویی در باتری)، فشردهسازی هوشمند تصاویر و ریکوردرهای سبکتر. در ادامه، دامنهی کاربرد از Small Bowel Capsule فراتر رفت و کپسول مری و سپس کپسول کولون معرفی شد تا تصویربرداری از روده بزرگ برای غربالگری ضایعات کوچک و پولیپها نیز ممکن شود.
در میانهی دههی ۲۰۱۰، منظرهی رقابتی تغییر کرد: Given Imaging ابتدا به Covidien و سپس به Medtronic پیوست تا توسعهی PillCam با پشتوانهی مهندسی و بازار گستردهتری ادامه یابد. همزمان، بازیگران دیگری مانند CapsoVision با CapsoCam وارد میدان شدند و معماری متفاوتی ارائه کردند (ذخیرهسازی مبتنی بر کپسول و بازیابی پس از دفع یا راهکارهای انتقال دادهی ترکیبی). در شرق آسیا، فناوری کپسولهای کنترلشونده با میدان مغناطیسی مطرح شد؛ پزشک با یک کنترلر مغناطیسی خارجی میتواند هدایت دید را بهبود دهد و از نقاط کلیدی معده یا ابتدای رودهها تصویربرداری هدفمندتری بگیرد—گامی مهم برای رفع یکی از محدودیتهای «عبور пасیو» در کپسولهای کلاسیک.
با بلوغ سختافزار، تمرکز صنعت به سمت نرمافزار و الگوریتم چرخید. نسلهای جدید، از هوش مصنوعی و سامانههای کمکتشخیصی (CADx/CADe) برای پیشاولویتبندی فریمها، تشخیص خودکار پولیپ، زخم، آنگیودیسپلازی و برچسبگذاری رویدادها بهره میبرند. این جهش نرمافزاری، زمان بازبینی پزشک را کاهش و حساسیت تشخیصی را در بیماران مناسب افزایش داده است. از سوی دیگر، باتریهای کممصرفتر و مدارهای تصویربرداری پیشرفته، زمان پایش را طولانیتر و نرخ تصاویر غیرقابلاستفاده را کمتر کردهاند.

دستگاه آنالیز کپسول آندوسکوپی
همهگیری کووید-۱۹ نیز روندی تازه ساخت: پروتکلهای بلع در منزل (At-home ingestion) با نظارت از راه دور مطرح شد تا دسترسی بیماران مناطق دورافتاده یا افراد با محدودیت حرکتی افزایش یابد. این تجربه نشان داد کپسول آندوسکوپی خانگی میتواند بخشی از مراقبتهای استاندارد شود، بهویژه وقتی انتقال بیسیم امن، اپلیکیشنهای بیمار و داشبوردهای پزشک یکپارچه باشند.
امروز، تاریخچهی کپسول آندوسکوپی از «PillCamِ اولیه» به اکوسیستم متنوعی رسیده است: کپسولهای اختصاصی برای روده باریک، کولون و مری؛ نسخههای کنترلمغناطیسی؛ رکوردرهای سبک با ارتباط ابری؛ و الگوریتمهای AI که به چشم پزشک قدرت بیشتری میدهند. فردا چه؟ نقشهی راه پژوهشها به سمت بیوپسیهای مینیاتوری، حسگرهای چندوجهی، دارورسانی هدفمند و ناوبری دقیقتر است. بدین ترتیب، تاریخچهی کپسول آندوسکوپی فقط مرور گذشته نیست؛ پیشنویس آیندهی آندوسکوپی بدون درد و کمعارضه است که هر سال با نوآوریهای اپتیکی، الکترونیکی و هوشمند، به واقعیت نزدیکتر میشود.
آندوسکوپی کپسولی از بیرون چیزی جز یک قرص هوشمند نیست، اما درون آن یک زنجیرهی کامل تصویربرداری پزشکی فشرده شده است. بدنهی کپسول از پلیمرهای زیستسازگار ساخته میشود و یک پنجرهی نوری شفاف دارد. پشت این پنجره، لنز اپتیکی با عمق میدان کوتاه و یک حسگر CMOS قرار گرفته که با LEDهای سفید کممصرف روشن میشود. مجموعهی حسگر–لنز برای مشاهدهی مخاط روده در فاصلهی نزدیک بهینه شده؛ میدان دید (FOV) در نسلهای جدید گستردهتر شده و اعوجاج لبهها با پردازش نرمافزاری تصحیح میشود تا جزئیات ظریف ضایعات کوچک از دست نرود.
قلب پردازش داخل کپسول یک ASIC/MCU کممصرف است که وظیفهی کنترل نوردهی (Auto-Exposure)، تعادل رنگ سفید (AWB)، فشردهسازی تصویر و مدیریت انرژی را بر عهده دارد. برای کاهش مصرف باتری، کپسولها از نرخ فریم تطبیقی استفاده میکنند: در مسیرهای یکنواخت، فریمریت پایین میآید و هنگام حرکت سریع یا ورود به ناحیهی مشکوک، بالا میرود. این «وظیفهچرخهای» (Duty Cycling) همراه با فشردهسازی کارآمد، زمان تصویربرداری را افزایش میدهد و نویز را در شرایط نوری پایین مهار میکند. در برخی مدلهای کولون، دو دوربین در دو سر کپسول نصب است تا میدان دید همپوشان ایجاد شود و احتمال جاافتادگی ضایعات کاهش یابد.
توان کپسول از باتریهای لیتیومی اولیهی بسیار کوچک تأمین میشود. بهدلیل محدودیت حجم (تقریباً در ابعاد 11×26 میلیمتر و وزنی چند گرم)، هر میلیوات اهمیت دارد. از اینرو، تمام اجزا—از LEDها تا کُدِک تصویر—برای مصرف فوقالعاده پایین طراحی میشوند. دادهها از طریق پیوند بیسیم باند ISM با تصحیح خطا (FEC) به ریکوردر پوشیدنی (کمربندی/چسبی) منتقل میشوند. ریکوردر، سیگنال را ذخیره و معمولاً بهصورت امن رمزگذاری میکند تا بعدها به ایستگاه پزشک یا PACS/Cloud منتقل شود. برخی سامانهها با آنتنهای چندگانهی خارجی شدت سیگنال را ثبت میکنند تا مکانیابی نسبی کپسول و تخمین زمان عبور از سگمنتهای روده ممکن شود.
کیفیت تصویر فقط به سختافزار وابسته نیست؛ pipeline نرمافزاری نقش کلیدی دارد. الگوریتمهای کاهش نویز، افزایش کنتراست و شارپسازی موضعی، بافتهای صاف و زخمهای ظریف را برجستهتر میکنند. در مرحلهی بازبینی، هوش مصنوعی (CADe/CADx) فریمها را اولویتبندی میکند، نشانههای پولیپ، آنگیودیسپلازی، زخم و خونریزی را برجسته میسازد و زمان مرور پزشک را بهطور محسوسی کاهش میدهد؛ در عین حال، تصمیم نهایی همچنان با پزشک است. برای معده یا کولون، برخی سامانهها از کنترل مغناطیسی خارجی استفاده میکنند تا جهتگیری کپسول تغییر کند و هدایت دید هدفمند به دست آید—پاسخی به محدودیت «حرکت پسیو» با پریستالسیس.
زیرساخت آمادگی بیمار نیز بخش مهمی از مبانی علمی است. برای کوچککردن آرتیفکتها، معمولاً ناشتایی، پاکسازی روده با محلولهای پلیاتیلن گلیکول و مصرف سیمتیکون (کاهندهی کف) توصیه میشود تا SNR تصویری بالا رود. در بیماران با احتمال تنگی، ابتدا Patency Capsule (کپسول عبوریِ قابلحل) بهکار میرود تا ریسک گیرکردن ارزیابی شود. موارد پرهیز شامل انسداد یا تنگی شناختهشده، اختلال شدید بلع و انجام MRI تا قبل از خروج کپسول است. دربارهی تداخل تجهیزات قابل کاشت (مثل ضربانساز)، بسته به سازنده و نسل دستگاه، ارزیابی فردی لازم است.
از منظر یکپارچهسازی بالینی، سامانههای جدید با استانداردهای تبادل داده (مانند DICOM/HL7 در سطح سامانهی اطلاعات بیمارستانی) سازگار میشوند تا گزارش ساختاری و خروجیهای تصویری بهسادگی وارد پروندهی الکترونیک سلامت شود. امنیت دادهها (رمزنگاری لینک بیسیم و دیسک) برای حریم خصوصی بیمار حیاتی است، بهویژه در پروتکلهای بلع در منزل که داده از راه دور منتقل میشود.
در نهایت، مبانی تکنولوژیک کپسول آندوسکوپی ندوسکوپی کپسولی بر سه ستون استوار است: اپتیک و حسگر بهینهشده برای فاصلهی نزدیک، الکترونیک کممصرف با مخابرات مقاوم، و هوش نرمافزاری برای ارتقای کیفیت و کارایی تشخیصی. پیوند این سه، تصویربرداری گسترده و کمعارضه از دستگاه گوارش را ممکن کرده و مسیر را برای نسلهای بعدی—از بیوپسی مینیاتوری تا دارورسانی هدفمند و ناوبری دقیق—هموار میسازد. این همان زیربنای علمی است که آندوسکوپی کپسولی را به «آیندهی آندوسکوپی بدون درد و کمعارضه» نزدیک میکند.
آندوسکوپی کپسولی در عمل یک خانواده از ابزارهای تشخیصی است که با توجه به بخشهای مختلف دستگاه گوارش و سناریوهای بالینی، طراحیهای متفاوتی دارد. شناخت این انواع به انتخاب درست بیمار، آمادهسازی مناسب و بهینهسازی دقت تشخیص کمک میکند.
الف) آندوسکوپی کپسولی روده باریک (SBCE) – Small Bowel Capsule Endoscopy
پرکاربردترین نوع است. برای ارزیابی خونریزی گوارشی پنهان، کمخونی فقر آهن با منشأ نامشخص، بیماری سلیاک و بیماریهای التهابی روده (IBD) در ژژunum و ایلئوم استفاده میشود. لنز و حسگر برای تصویربرداری نزدیک از مخاط روده باریک بهینه شدهاند؛ معمولاً نرخ فریم تطبیقی و الگوریتمهای کاهش نویز دارند تا با مصرف پایین باتری، طول مسیر طولانی را پوشش دهند. در بیماران مشکوک به تنگی، پیش از SBCE از Patency Capsule (کپسول عبوری قابلحل) برای کاهش ریسک گیرکردن استفاده میشود.
ب) آندوسکوپی کپسولی کولون (CCE) – Colon Capsule Endoscopy
برای غربالگری پولیپها و ارزیابی روده بزرگ در بیمارانی که کولونوسکوپی استاندارد برایشان دشوار یا ناتمام مانده است بهکار میرود. کپسول کولون اغلب دوربین دوطرفه و میدان دید گسترده دارد تا احتمال جاافتادن ضایعات کاهش یابد. نقطهی کلیدی در CCE کیفیت آمادهسازی کولون است: رژیم پاکسازی دقیق، محرکهای حرکتی و زمانبندی دقیق بلع برای بهحداقل رساندن باقیماندههای مدفوع و بالا بردن حساسیت تشخیص حیاتی است. مزیت CCE راحتی بیمار و نبودِ نیاز به آرامبخشی است؛ محدودیت آن عدم امکان بیوپسی یا پولیپبرداری در همان جلسه است.
پ) کپسول آندوسکوپی مری (ECE) – Esophageal Capsule
برای ارزیابی سریع مری در شرایطی مثل مری بارت، واریس مری یا ریفلاکس مقاوم به درمان استفاده میشود. چون زمان عبور کپسول از مری کوتاه است، برخی طراحیها نرخ فریم بالاتر یا پروتکلهای خاص بلع (مانند دراز کشیدن و بلع مرحلهای) را بهکار میگیرند تا پوشش تصویری کافی حاصل شود. ECE بهویژه در غربالگری غیرتهاجمی و پیگیری بیمارانی که تحمل آندوسکوپی انعطافپذیر را ندارند مفید است.
ت) کپسولهای معده و کپسولهای کنترلمغناطیسی (MCE)
مشاهدهی معده بهدلیل حجم بالا و چینهای متعدد چالشبرانگیز است. راهحل، کنترل مغناطیسی خارجی است: پزشک با یک کنترلر مغناطیسی جهتگیری کپسول را تغییر میدهد تا نواحی کلیدی (آنتروم، تنه، فوندوس، پیلور) بهتر دیده شوند. این رویکرد برای معده و ابتدای روده باریک، هدایت دید هدفمند ایجاد میکند و بر محدودیت «حرکت پسیو با پریستالسیس» غلبه میکند. کیفیت آمادهسازی (مایعات شفاف، سیمتیکون برای کاهش کف) در این نوع اهمیت دوچندان دارد.
ث) کپسولهای اختصاصی و سناریوهای خاص
ج) آندوسکوپی کپسولی در منزل (At-home ingestion)
در مراکز دارای زیرساخت، بلع کپسول میتواند تحت نظارت از راه دور انجام شود. رکوردر پوشیدنی دادهها را ذخیره و بهصورت امن به کلینیک ارسال میکند. این مدل، دسترسی بیماران مناطق دورافتاده یا افراد با محدودیت حرکتی را افزایش میدهد و با پروتکلهای سئوپذیر «کپسول آندوسکوپی در منزل» به عنوان یک کلیدواژهی رو به رشد، توجه زیادی جلب کرده است.
چ) تفاوتهای فنی میان انواع
جمعبندی انتخاب نوع مناسب
اگر هدف خونریزی پنهان یا IBD روده باریک است، SBCE گزینهی اول است؛ برای غربالگری یا تکمیل ارزیابی کولون، CCE با آمادهسازی دقیق توصیه میشود؛ برای غربالگری مری یا پیگیری بارت، ECE مناسب است؛ و در مطالعهی معده یا هدایت هدفمند، کپسولهای کنترلمغناطیسی ارزش افزوده میدهند. این تقسیمبندی، مسیر شخصیسازی کپسول آندوسکوپی را هموار میکند و به آیندهی آندوسکوپی بدون درد و عوارض نزدیکترمان میسازد.

pill camکپسول آندوسکوپی
آندوسکوپی کپسولی وقتی بیشترین ارزش را دارد که پرسش بالینیِ «کجاست منبع ضایعه یا خونریزی؟» با روشهای مرسوم بیپاسخ مانده باشد، یا بیمار تحمل آندوسکوپی تهاجمی را نداشته باشد. اندیکاسیونها برحسب ناحیه هدف (روده باریک، کولون، مری) کمی فرق میکند، اما در همه موارد هدف، تصویربرداری غیرتهاجمی، گسترده و بیمارپسند است.
الف) روده باریک (Small Bowel Capsule Endoscopy – SBCE)
ب) کولون (Colon Capsule Endoscopy – CCE)
نکته: موفقیت CCE به آمادگی دقیق روده (کلینزینگ + زمانبندی محرکها) وابسته است و برخلاف کولونوسکوپی، بیوپسی/درمان همزمان نمیدهد.
پ) مری (Esophageal Capsule Endoscopy – ECE)
چون عبور کپسول از مری سریع است، نرخ فریم بالا و پروتکل بلع هدفمند برای پوشش کافی لازم است.
ت) سناریوهای انتخاب بیمار و مسیرهای تصمیمگیری
ث) چه زمانی مناسب نیست؟ (تمایز اندیکاسیون از احتیاط)
جمعبندی سئویی: اگر بهدنبال «آندیکاسیونهای آندوسکوپی کپسولی» هستید، سه خوشه اصلی را به خاطر بسپارید: OGIB/IDA نامشخص، IBD/کرون روده باریک، و کولونوسکوپی ناقص یا غربالگری غیرتهاجمی کولون. افزودن ECE برای مری بارت و استفاده در کودکان نیز دامنهی کاربرد را کامل میکند. انتخاب درست بیمار، کلید حداکثرسازی دقت و حداقلسازی عارضه در مسیر آندوسکوپی بدون درد و کمخطر است.
کپسول آندوسکوپی بهعنوان یک فناوری غیرتهاجمی، در بسیاری از سناریوها مزیتهای روشنی نسبت به آندوسکوپی سنتی (اندوسکوپی فوقانی و کولونوسکوپی) دارد. این مزیتها هم از منظر راحتی و ایمنی بیمار قابل توجهاند و هم از نظر کارایی تشخیصی و بهرهوری سیستم درمانی.
راحتی و تجربه بیمار: بزرگترین مزیت، حذف لولهگذاری و بیهوشی/آرامبخشی است. بیمار تنها یک کپسول به اندازهی ویتامین میبلعد و فعالیت روزمرهاش تقریباً مختل نمیشود؛ دوره نقاهت نزدیک به صفر است و خبری از گلودرد، نفخ یا ناراحتیهای پس از آندوسکوپی کلاسیک نیست. برای افراد سالخورده، بیماران پرریسک بیهوشی، کودکان، و کسانی که اضطراب روشهای تهاجمی را دارند، این تفاوت بهمعنای پذیرش درمانی بالاتر و پایبندی بهتر به مسیر تشخیصی است.
ایمنی و ریسک پایینتر عوارض: در آندوسکوپی سنتی—هرچند نادر—خطراتی مانند خونریزی ناشی از مداخله، پرفوراسیون، عوارض داروهای آرامبخش و انتقال عفونت وجود دارد. آندوسکوپی کپسولی بهدلیل ماهیت غیرتهاجمی، این ریسکها را بهطور چشمگیری کاهش میدهد. تنها عارضهی خاص آن گیرکردن کپسول در تنگیهاست که با غربالگری قبلی (Patency Capsule) و انتخاب دقیق بیمار، مدیریتپذیر میشود. همچنین تا خروج کپسول، انجام MRI ممنوع است که با اطلاعرسانی درست قابل پیشگیری است.
کارایی تشخیصی در روده باریک: آندوسکوپی سنتی دسترسی محدودی به روده باریک دارد؛ اما کپسول آندوسکوپی مسیر کامل روده باریک را با میدان دید وسیع میبیند. در خونریزی گوارشی پنهان (OGIB) و کمخونی فقر آهن با منشأ نامشخص—وقتی اندوسکوپی فوقانی و کولونوسکوپی طبیعیاند—کپسول میتواند ضایعاتی مانند آنگیودیسپلازی، زخمها یا ضایعات کوچک را آشکار کند و مسیر درمان را هدفمند سازد. در IBD (بهویژه کرونِ روده باریک)، این روش برای ارزیابی فعالیت مخاطی و پایش پاسخ به درمان ارزشمند است.
دسترسی و انعطافپذیری بیشتر: با فراهم شدن پروتکلهای بلع در منزل و ریکوردرهای پوشیدنی متصل به اَپ، بیماران مناطق دورافتاده یا افراد با محدودیت حرکتی نیز از خدمات تشخیصی باکیفیت بهرهمند میشوند. این مدل، عدالت در سلامت را بهبود میدهد و بار مراجعات حضوری غیرضروری را کاهش میدهد.
بهرهوری سیستم و هزینهاثربخشی: حذف آرامبخشی، منابع اتاق اندوسکوپی و ریکاوری، باعث افزایش ظرفیت مراکز و کاهش هزینههای غیرمستقیم (مرخصی از کار، همراه، رفتوآمد) میشود. در سطح کلینیک، زمان پزشک برای بازبینی با کمک هوش مصنوعی (CADe/CADx) کاهش مییابد؛ الگوریتمها فریمهای مشکوک به پولیپ، زخم، خونریزی یا آنگیودیسپلازی را برجسته و اولویتبندی میکنند و کیفیت گزارش را یکنواختتر میسازند. یکپارچگی با PACS/EMR (خروجی DICOM، گزارش ساختاری) گردش کار را ساده میکند.
پذیرش بیمار و تجربه کاربر: نبودِ قطعه بیرونی (در برخی سیستمها) و طراحی سبک ریکوردر به راحتی روزمره کمک میکند. آمادگی بیمار نیز معمولاً سادهتر از کولونوسکوپی است—بهخصوص در SBCE که تمرکز بر کاهش کف (سیمتیکون) و شفافسازی مایعات است. در CCE (کپسول کولون) کیفیت پاکسازی همچنان حیاتی است، اما در ازای آن راحتی و عدم نیاز به آرامبخشی تجربه مثبتتری ایجاد میکند؛ بهخصوص برای بیمارانی که کولونوسکوپی کامل برایشان دشوار یا نامطلوب است.
شخصیسازی مسیر تشخیص: کپسول آندوسکوپی میتواند نقش تریاژ ایفا کند: ابتدا منبع ضایعه را دقیقتر مشخص میکند و سپس در صورت نیاز، آندوسکوپی مداخلهای هدفمند انجام میشود. این رویکرد از مداخلات غیرضروری میکاهد و زمان تا درمان قطعی را کوتاه میکند.
هرچند کپسول آندوسکوپی راهی غیرتهاجمی و بیمارپسند برای تصویربرداری از دستگاه گوارش است، اما مثل هر فناوری پزشکی، مجموعهای از محدودیتها و چالشها دارد که در انتخاب بیمار، تفسیر نتایج و طراحی مسیر درمان باید بهصورت شفاف در نظر گرفته شوند.
۱) تشخیصی، نه درمانی
مهمترین محدودیت این است که کپسول فقط تصویر میگیرد؛ بیوپسی، پولیپبرداری، هموستاز یا دیلاتاسیون در همان جلسه ممکن نیست. بنابراین در صورت کشف ضایعه، بیمار معمولاً به آندوسکوپی مداخلهای برگشت میخورد؛ این یعنی یک مرحلهی اضافی، هزینه و زمان بیشتر.
۲) خطر گیرکردن کپسول (Capsule Retention)
در تنگیها یا狭窄 ناشی از کرون، تومور، چسبندگی، انتروپاتی NSAID یا پرتودرمانی امکان ماندگاری کپسول وجود دارد. هرچند شیوع کلی پایین است، اما در بیماران پرخطر باید قبل از SBCE از Patency Capsule استفاده شود. مدیریت ریتنشن بسته به محل میتواند اندوسکوپیک یا جراحی باشد.
۳) وابستگی به آمادگی و فاکتورهای فنی
کیفیت تصویر به آمادگی روده (پاکسازی، کاهش کف با سیمتیکون، ناشتایی) و پوزیشن/حرکت بستگی دارد. در کولون کپسل (CCE)، هر نقص در کلینزینگ، حساسیت تشخیص را کم میکند. در کپسول مری (ECE)، زمان عبور کوتاه خطر جاافتادن ضایعات را بالا میبرد و نیاز به نرخ فریم بالاتر یا پروتکلهای بلع دارد. در معده، حجم و چینهای متعدد باعث دشواری پوشش کامل میشود و حتی با کنترل مغناطیسی نیز اپراتور به مهارت نیاز دارد.
۴) محدودیتهای لوکالیزیشن و زمان عبور
کپسول نقشهی دقیق سهبعدی ارائه نمیدهد؛ محل ضایعه معمولاً تخمینی (بر اساس زمان عبور، شدت سیگنال آنتنها یا نشانههای آناتومیک) گزارش میشود. گذر بیش از حد سریع یا کند از سگمنتها، یا تأخیر معدی/کولونیک میتواند منجر به مطالعهی ناقص شود (مثلاً باتری تمام شود قبل از اتمام مسیر).
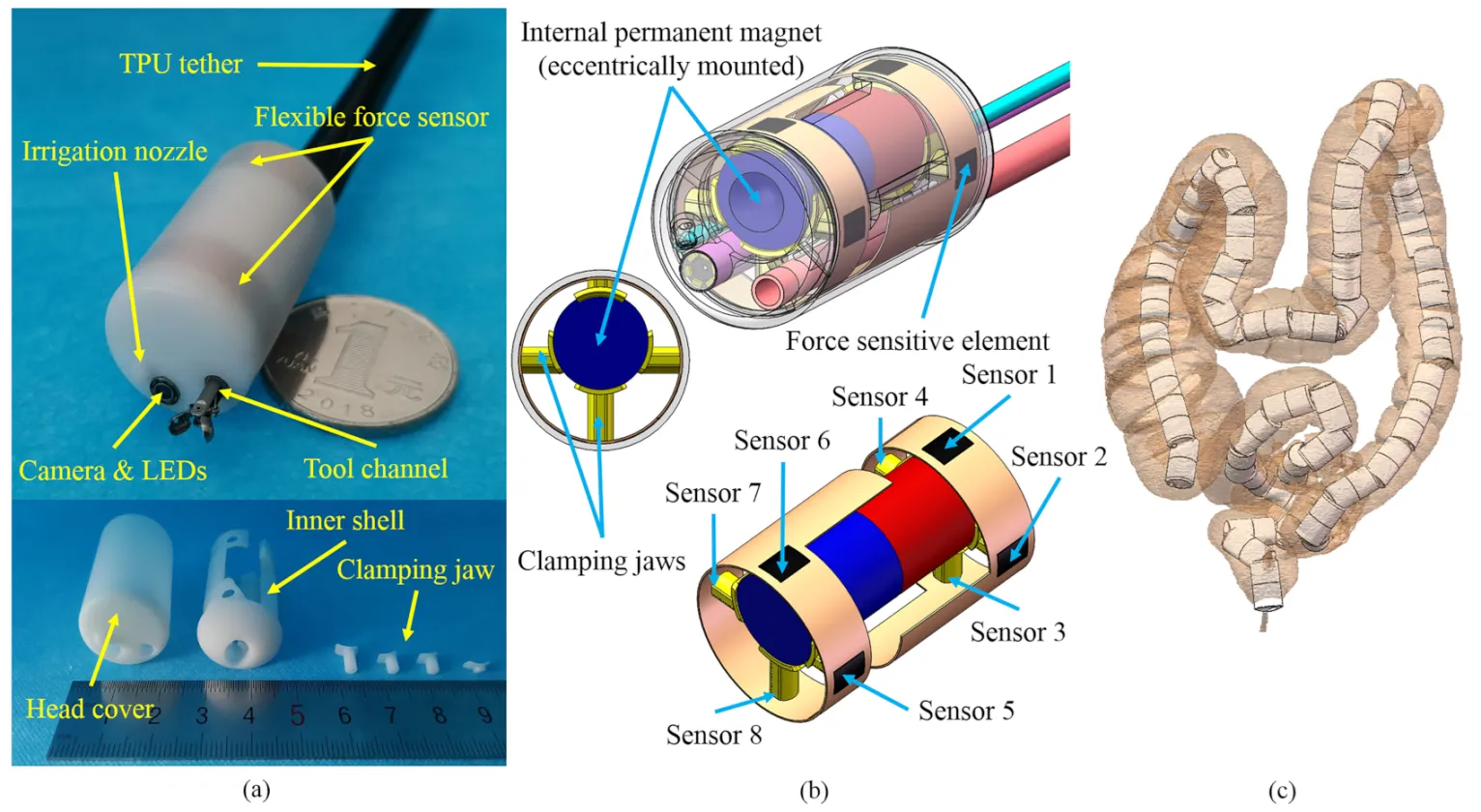
ساختار کپسول آندوسکوپی
۵) خطاهای تفسیر (False Positive/Negative)
کف، صفرا، مواد غذایی باقیمانده و بازتاب نور میتواند شبیه پولیپ یا خون دیده شود. در مقابل، ضایعات تخت کوچک یا خونریزی متناوب ممکن است جا بیفتند. هوش مصنوعی در آندوسکوپی کپسولی (CADe/CADx) زمان مرور را کم میکند، اما جایگزین قضاوت بالینی نیست و امکان over-call یا under-call وجود دارد.
۶) تداخلات و موارد منع نسبی
تا زمان دفع کپسول، MRI ممنوع است. در بیماران دارای پیسمیکر/ICD یا ایمپلنتهای الکترونیکی، بسته به نسل دستگاه و سازنده، باید ارزیابی فردی انجام شود. در اختلال بلع، انسداد شناختهشده، بارداری پرخطر یا ناتوانی در همکاری، احتمالاً روش مناسبتری لازم است.
۷) بارِ داده و نیاز به زیرساخت
هر مطالعه هزاران فریم تولید میکند. بدون سیستم بازبینی کارآمد، مانیتورهای مناسب و آرشیو امن (PACS/Cloud)، بهرهوری کاهش مییابد. حریم خصوصی داده در مدلهای بلع در منزل و انتقال ابری باید با رمزنگاری و سیاستهای شفاف تضمین شود.
۸) اقتصاد سلامت و بازپرداخت
هزینهی دستگاهها و رکوردرها، قراردادهای سرویس و الگوریتمهای بازپرداخت بیمه در کشورها متفاوت است. اگرچه حذف آرامبخشی و اتاق اندوسکوپی میتواند هزینه-اثربخشی را بهبود دهد، اما در نبود پوشش بیمهای مناسب، دسترسی محدود میشود.
۹) استانداردسازی و منحنی یادگیری
پروتکلهای آمادهسازی، زمانبندی، کلینزینگ و گزارشنویسی ساختاری باید استاندارد شوند تا نتایج بین مراکز قابل مقایسه باشد. همچنین کنترل مغناطیسی و بازبینی مبتنی بر AI نیازمند آموزش هدفمند است.
۱۰) مخاطرات بالینی خاص
در خونریزی فعال ممکن است زمانبندی مطالعه با فاز خونریزی هماهنگ نشود و منبع دیده نشود. در IBD استنوزان، حتی با Patency Capsule نیز باید احتیاط کرد. در کودکان خردسال یا بیماران نورولوژیک، گاهی جاگذاری با آندوسکوپ ترجیح داده میشود.
جمعبندی سئویی: برای جستوجوهای «محدودیتهای آندوسکوپی کپسولی» و «چالشهای Capsule Endoscopy» به یاد داشته باشید: عدم امکان درمان همزمان، خطر گیرکردن کپسول، وابستگی شدید به آمادگی روده، محدودیت لوکالیزیشن، تداخل با MRI، نیاز به زیرساخت داده و بازپرداخت بیمهای. مدیریت این چالشها با انتخاب صحیح بیمار، Patency Capsule، پروتکلهای استاندارد، آموزش کاربر و بهرهگیری مسئولانه از AI، کلید دستیابی به تشخیص دقیق با حداقل عارضه و حرکت به سوی آندوسکوپی بدون درد و کمخطر است.
کپسول آندوسکوپی طی چند سال اخیر جهشهای بزرگی را تجربه کرده که آن را بیش از گذشته به رؤیای «آندوسکوپی بدون درد و عوارض» نزدیک کرده است. این پیشرفتها در سه لایهی اصلی رخ دادهاند: اپتیک و الکترونیک کممصرف، هوش مصنوعی و نرمافزار، و ناوبری/Workflow بالینی. نتیجه، افزایش دقت تشخیص، پوشش دید بهتر، کاهش زمان بازبینی و تجربهای بیمارمحورتر است.
۱) اپتیک پیشرفته و حسگرهای نسل جدید
لنزهای با میدان دید وسیعتر (Wide FOV) و حسگرهای CMOS نویزکم، جزئیات مخاطی روده باریک و کولون را بهتر نشان میدهند. نورپردازی LED کممصرف با کنترل خودکار نوردهی (Auto-Exposure) و تعادل رنگ سفید، ثبات رنگ و کنتراست را در شرایط نوری دشوار حفظ میکند. در کپسول کولون، استفاده از دوربینهای دوطرفه و همپوشانی میدان دید، احتمال جاافتادن پولیپهای تخت را کاهش داده است.
۲) مدیریت انرژی و نرخ فریم تطبیقی
باتریهای کوچکتر با راندمان بالاتر، همراه با Duty Cycling هوشمند و نرخ فریم تطبیقی (افزایش فریم در نواحی مشکوک/حرکت سریع و کاهش در مسیرهای یکنواخت) باعث شده زمان تصویربرداری طولانیتر و خروجی پایدارتر شود. این مهم، احتمال اتمام باتری پیش از تکمیل مسیر را کم میکند و کیفیت مطالعهی SBCE و CCE را بالا میبرد.
۳) کنترل مغناطیسی و ناوبری هدفمند
چالش «حرکت پسیو با پریستالسیس» با کنترل مغناطیسی خارجی تا حدی رفع شده است. در معده و ابتدای روده، پزشک میتواند با تغییر جهتگیری کپسول، نواحی کلیدی (فوندوس، آنتروم، پیلور) را هدفمند بررسی کند. این ناوبری، کیفیت ارزیابی معده و کپسول کولون را ارتقا میدهد و نیاز به تکرار مطالعه را کاهش میدهد.
۴) هوش مصنوعی در آندوسکوپی کپسولی (CADe/CADx)
الگوریتمهای یادگیری عمیق اکنون فریمها را اولویتبندی و نشانههای پولیپ، آنگیودیسپلازی، زخم، خون و الگوهای IBD را برجسته میکنند. این کار، زمان بازبینی پزشک را کاهش میدهد و حساسیت تشخیص را در بیماران منتخب افزایش میدهد. مدلهای جدید False Positive را با ترکیب زمینههای زمانی (Temporal Context) و «امتیاز اطمینان» محدود میکنند تا قضاوت بالینی سهیلتر شود. هوش مصنوعی همچنین میتواند کیفیت پاکسازی را بهصورت خودکار درجهبندی کند.
۵) یکپارچگی داده و ابر (Cloud)
رکوردرهای پوشیدنی جدید، انتقال امن به PACS/Cloud و صدور خروجی DICOM/HL7 را ساده کردهاند. داشبوردهای مبتنی بر وب با گزارشهای ساختاری، همکاری تیمی و پیگیری طولانیمدت را تسهیل میکنند. در پروتکلهای بلع در منزل (At-home ingestion)، رمزنگاری سرتاسری و ثبت رخدادها (Audit Trail) حریم خصوصی بیمار را تضمین میکند.
۶) آمادهسازی هوشمند و پروتکلهای بیمارمحور
ترکیب مایعات شفاف، سیمتیکون (کاهش کف) و زمانبندی محرکهای حرکتی، SNR تصویری را بهبود داده است. Patency Capsuleهای قابلحل با نشانگرهای زمانی/مکانی، غربالگری تنگی را دقیقتر کرده و ریسک گیرکردن کپسول را پایین آوردهاند. اپلیکیشنهای بیمار، گامبهگام آمادهسازی را هدایت و پایبندی را افزایش میدهند.
۷) چندحسگری و آیندهی مداخلات کمتهاجمی
پژوهشهای نوظهور به سمت حسگرهای چندگانه (pH، دما، امپدانس، مارکرهای التهابی) و تصویربرداری چندطیفی میروند تا تمایز بافتی بهتر و تشخیص زودهنگام ممکن شود. ایدههای در حال توسعه شامل بیوپسی مینیاتوری، دارورسانی هدفمند و لوازم جانبی رباتیک نرم است که میتواند مرز «صرفاً تشخیصی» بودن را جابهجا کند.
۸) اقتصاد سلامت و بازپرداخت هوشمند
با حذف آرامبخشی و اتاق ریکاوری، هزینههای غیرمستقیم کاهش یافته و مراکز میتوانند ظرفیت بیشتری را پوشش دهند. مدلهای بازپرداخت مبتنی بر ارزش (Value-Based) در حال شکلگیریاند؛ وقتی کپسول نقش تریاژ ایفا کند و آندوسکوپی درمانی را هدفمند سازد، «هزینه–اثربخشی» بهبود مییابد.
۹) استانداردسازی و آموزش مبتنی بر داده
قالبهای گزارش ساختاری، امتیازدهی مخاطی، و مسیرهای خوانش پلهای با چکلیستهای AI-Assisted در حال استاندارد شدناند. شبیهسازهای نرمافزاری و بانکهای فریم برچسبخورده، منحنی یادگیری را کوتاه و واریانس بینخوانندهای را کم میکنند.
آینده آندوسکوپی کپسولی با همگرایی سختافزارهای کوچکمصرف، هوش مصنوعی، ناوبری کنترلمغناطیسی و زیرساختهای ابری رقم میخورد؛ مسیری که آندوسکوپی را بهسمت تشخیص بدون درد و عوارض و هوشمند میبرد. این آینده را میشود در سه افق زمانی دید: نزدیکمدت (۱–۳ سال)، میانمدت (۳–۵ سال) و بلندمدت (۵–۱۰ سال).
در افق نزدیکمدت، انتظار میرود پروتکلهای بلع در منزل (At-home ingestion) با اپهای راهنمای بیمار و رکوردرهای ایمن، از خدمات مکمل به گزینهای استاندارد تبدیل شوند؛ بهخصوص برای OGIB/IDA نامشخص و بیماران پرریسک بیهوشی. الگوریتمهای CADe/CADx بلوغ بیشتری مییابند: اولویتبندی فریمها، امتیازدهی خودکار کیفیت پاکسازی، و تشخیص الگوهای ظریف (پولیپ تخت، آنگیودیسپلازی کمکنتراست) سریعتر و پایدارتر میشود. در همین بازه، مدلهای هزینه–اثربخشی و بازپرداخت مبتنی بر ارزش (Value-Based) در مسیرهای تریاژ جا میافتند: ابتدا کپسول محل ضایعه را مشخص میکند، سپس اندوسکوپی درمانی هدفمند انجام میشود؛ نتیجه، کاهش مداخلات غیرضروری و صرفهجویی منابع است.
در افق میانمدت، کنترل مغناطیسی از یک ویژگی ممتاز به جریان غالب در معده و کولون بدل میشود؛ پزشک با جویاستیک میدان دید را هدایت میکند و پوشش نواحی دشوار بهبود مییابد. سامانههای «Cloud-first» با خروجی DICOM/HL7-FHIR بهطور بومی با EMR/PACS یکپارچه میشوند؛ گزارشهای ساختاری، امتیاز فعالیت مخاطی و پیشنهادهای AI-Assisted در یک داشبورد واحد دیده میشود. در این دوره، شاخصهای کیفیت ویژه آندوسکوپی کپسولی تثبیت میشوند: «Time-in-View»، درصد پوشش سگمنتها، و معیارهای استاندارد پاکسازی معادل نمرههای کولونوسکوپی. آموزش هم دگرگون میشود: نمونهبانکهای فریم برچسبخورده، شبیهسازهای مرور و چکلیستهای هوشمند، واریانس بینخوانندهای را کاهش میدهد. از منظر امنیت و حریم خصوصی، «Privacy-by-Design» و گواهینامههای امنیت سایبری (برای لینک بیسیم و ابر) پیشنیاز استقرار گسترده خواهد بود.
افق بلندمدت جایی است که کپسولها از «صرفاً تشخیصی» عبور میکنند. پژوهشها بهسمت کپسولهای چندمنظوره میرود:
اینها آغازگر عصر «ترانوستیک» (تشخیص+درمان) در قالب قرص خواهند بود. همزمان، ادغام کپسول آندوسکوپی با مسیرهای غربالگری جمعیتی (مثلاً پس از FIT مثبت یا در کنار Liquid Biopsy) تریاژ هوشمند را تقویت میکند: ابتدا غربالگری ارزان و دردسترس، سپس کپسول برای تعیین محل، و در نهایت مداخله هدفمند.
در سطح سیستم سلامت، سلامت از راه دور (Tele-GI) و کلینیکهای مجازی مرور کپسول، دسترسی مناطق کمبرخوردار را ارتقا میدهند و شکاف نابرابری را میبندند. پایداری محیطزیستی بهعنوان معیار نوظهور وارد طراحی میشود: پلیمرهای زیستسازگار، کاهش حجم پسماند، و چرخههای بازیافت برای رکوردرها. از سوی دیگر، مسیرهای قانونگذاری برای SaMD (نرمافزار بهعنوان وسیله پزشکی) و الگوریتمهای یادگیرنده نیازمند شفافیت، مدیریت نسخه و Real-World Evidence هستند تا اعتماد بالینی و پوشش بیمهای را تضمین کنند.
جمعبندی: آیندهی آندوسکوپی کپسولی آیندهای چندحسی، متصل به ابر، هدایتپذیر و هوشمند است؛ از تشخیص بدون درد و عوارض امروز به ترانوستیک هدفمند فردا. هرچه کنترل مغناطیسی، AI، و حسگرهای چندوجهی بالغتر شوند، فاصلهی بین تشخیص و درمان کوتاهتر و تجربهی بیمار انسانمحورتر میشود. مسیر پیش رو روشن است: کاهش درد و عارضه، افزایش دقت و دسترسپذیری، و ارزشآفرینی برای بیمار و سیستم سلامت.

capsule endoscopy
کپسول آندوسکوپی امروز از یک ایده نو به یک ابزار بالینی بالغ رسیده است و مسیر «آندوسکوپی بدون درد و کمعارضه» را هموار میکند. این فناوری با تصویربرداری گسترده از روده باریک و، در مدلهای اختصاصی، از کولون و مری، شکافهای تشخیصی را وقتی روشهای کلاسیک پاسخ ندادهاند پُر میکند؛ بهویژه در خونریزی گوارشی پنهان (OGIB)، کمخونی فقر آهن نامشخص، سلیاک و IBD. مزیتهای کلیدی آن—راحتی بیمار، حذف آرامبخشی، کاهش عوارض تهاجمی، امکان بلع در منزل—با نوآوریهای اخیر مانند هوش مصنوعی (CADe/CADx)، کنترل مغناطیسی، باتریهای کممصرف و انتقال امن ابری تقویت شدهاند و حساسیت تشخیصی و بهرهوری مرور را بالا بردهاند.
با این حال، آندوسکوپی کپسولی هنوز جایگزین کامل آندوسکوپی مداخلهای نیست؛ زیرا بیوپسی، هموستاز یا پولیپبرداری در همان جلسه ممکن نیست و در تنگیها خطر گیرکردن کپسول وجود دارد. همچنین کیفیت خروجی به آمادهسازی دقیق (پاکسازی، کاهش کف با سیمتیکون، رعایت ناشتایی) وابسته است و لوکالیزیشن ضایعه غالباً نسبی است. بنابراین نگاه درست، همافزایی است: کپسول برای تریاژ هوشمند و تعیین محل/گستره ضایعه، و سپس مداخله هدفمند با روشهای سنتی.
توصیهها برای پزشکان (Clinicians):
توصیهها برای مدیران و سیاستگذاران سلامت:
توصیهها برای بیماران:
اولویتهای پژوهشی و آیندهنگری: